नेपालको औषधी नीति कहाँनिर कमजोर ?

नेपालमा औषधी नियमनको मुख्य आधार औषधी ऐन, २०३५ हो । यसको कार्यान्वयनका लागि औषधी दर्ता नियमावली- २०३८, औषधी जाँचबुझ तथा निरीक्षण नियमावली – २०४०, औषधी स्तर निर्धारण नियमावली- २०४३, औषधी विक्रीवितरण संहिता- २०८०, तथा आपतकालीन प्रयोग सम्बन्धी संहिता- २०७७ जस्ता साधनहरू प्रयोगमा छन्।
औषधी व्यवस्था विभाग (डीडीए)को आधिकारिक “Act, Regulations & Code” सूचीमा यी प्रमुख नियामक उपकरणहरू स्पष्ट देखिन्छन् र औषधी ऐनको संशोधित संस्करणसमेत हाल उपलब्ध छ।
मुख्य कमजोरीहरू
१. कानुनी आधार पुरानो, बजार आधुनिक
औषधि ऐन, २०३५ को मूल संरचना पुरानो समयको औषधी बजारलाई ध्यानमा राखेर बनेको हो। आजको बजारमा fixed-dose combinations (FDCs), modified-release formulations, biologics, supplements, promotional incentives, digital sales र जटिल supply chains प्रमुख बनिसकेका छन्; तर मूल कानुनी ढाँचा यिनलाई समग्र रूपमा समेट्ने गरी आधुनिक बनाइएको देखिँदैन। DDA ले ऐन संशोधन प्रकाशित गरे पनि संरचनागत रूपमा नियमन अझै धेरै हदसम्म परम्परागत औषधी नियन्त्रण मोडेलमै आधारित छ।
२. मूल्य नियन्त्रणको दायरा साँघुरो
नेपालमा MRP नियमन कानुनी रूपमा सम्भव भए पनि व्यवहारमा सीमित औषधी र सीमित formulation मा मात्र लागू हुने प्रवृत्ति देखिन्छ। यो समस्याको जड कानुनभन्दा पनि कानुनको प्रयोगको दायरा हो—अर्थात् selected molecules मा मूल्य तोक्ने, तर therapeutic substitutes वा FDC/modified-release formulations लाई बाहिर छोड्ने। यसले regulated र unregulated बजारबीच असमान खेलमैदान बनाउँछ। औषधी ऐनको ढाँचा र DDA का कोड/नियमहरूले मूल्य नियमन सम्भव बनाउँछन्, तर व्यापक, नियमित, evidence-based pricing system निर्माण गरेको स्पष्ट देखिँदैन।
३. नियमित मूल्य पुनरावलोकन (Revision) को स्पष्ट, बाध्यकारी प्रणाली कमजोर
कानुनले मूल्य तोक्न सक्ने अधिकार दिन्छ, तर कति अन्तरालमा पुनरावलोकन गर्ने, कुन आधारमा गर्ने, कसरी transparent बनाउने भन्ने पक्ष संस्थागत रूपमा बलियो छैन। यही कारण एक पटक तोकिएको मूल्य सूची बजार, मुद्रास्फीति, विनिमय दर, उत्पादन लागत र formulation shift अनुसार समयमै अद्यावधिक नहुन सक्छ। यसले नियमनलाई static बनाउँछ र उद्योगलाई unregulated products तर्फ सर्न प्रोत्साहन दिन्छ।
४. फार्मेसी तहमा गुणस्तर, भण्डारण र वितरणको नियम भए पनि कार्यान्वयन चुनौतीपूर्ण
DDA ले औषधी विक्रीवितरण संहिता, २०८० लागू गरेको छ र हाल Good Pharmacy Practice तथा Good Storage and Distribution Practice परिपालना सम्बन्धी सूचनासमेत जारी गरिरहेको छ। यसको अर्थ नियामक निकायले retail and distribution level governance लाई गम्भीरतापूर्वक लिन थालेको छ। तर नेपालमा प्रदेश/स्थानीय स्तरसम्म एकरूप अनुगमन, मानव स्रोत, निरीक्षणको नियमितता, र accountability अझै ठूलो चुनौती हो। नियम छ; तर सबै ठाउँमा समान कार्यान्वयन छैन।
५. निरीक्षण र enforcement बढी reactive, कम proactive
औषधी जाँचबुझ तथा निरीक्षण नियमावली, २०४० जस्ता कानुनी साधनहरूले निरीक्षणको आधार बनाउँछन्। तर व्यवहारमा धेरैजसो enforcement recall notice, urgent notice, बिक्री रोक्का, वा complaint-driven action मार्फत देखिन्छ। DDA वेबसाइटमा बारम्बार recall र urgent notice देखिनु एउटा सकारात्मक पारदर्शिता संकेत हो, तर यसले बजार अनुगमनको ठूलो हिस्सा अझै “समस्या भएपछि प्रतिक्रिया” मा निर्भर हुनसक्ने संकेत पनि दिन्छ।
६. झुट्टा/भ्रामक प्रचार नियन्त्रणको आधार भए पनि promotional regulation अझै संवेदनशील क्षेत्र
औषधी ऐनको प्रस्तावनाले नै झुट्टा वा भ्रमात्मक प्रचार रोक्ने उद्देश्य राखेको छ। DDA ले हालै झुट्टा, भ्रामक प्रचारप्रसार तथा विक्रीवितरणबारे जरुरी सूचनासमेत दिएको देखिन्छ। तर field reality मा prescriber influence, company promotion, brand pushing, therapeutic substitution को अस्पष्टता, र consumer information asymmetry जस्ता मुद्दा अझै संवेदनशील छन्। अर्थात् कानुनी intent छ, तर promotional ecosystem लाई पूर्ण रूपमा पारदर्शी र उत्तरदायी बनाउने institutional enforcement अझै अपर्याप्त देखिन्छ।
७. संघीय संरचनामा भूमिकाको स्पष्टता अझै विकासक्रममा
फार्मेसी दर्ता/नवीकरण सम्बन्धी प्रदेशस्तरीय सूचनाहरूले अब औषधी प्रशासन संघीय संरचनासँग समायोजन गरिरहेको देखाउँछ। तर यसले नयाँ चुनौती पनि ल्याउँछ: संघ, प्रदेश, स्थानीय तहबीच कसको काम के हो? अनुगमन, renewal, professional card, retail control, price monitoring, complaint handling—यी सबैमा एकरूपता नहुँदा regulatory fragmentation बढ्न सक्छ।
संक्षेपमा आलोचनात्मक निष्कर्ष
नेपालको औषधि नियमनको कानुनी हाड–मासु छ, तर स्नायु कमजोर भन्ने अवस्था छ। अर्थात्:
- ऐन छ
- नियमावली छ
- संहिता छ
- सूचनाहरू जारी हुन्छन्
तर प्रणालीगत कमजोरीहरू:
- दायरा साँघुरो
- revision अनियमित
- enforcement reactive
- promotional governance कमजोर
- federal coordination अपूरो
- formulation-level loopholes बाँकी
यही कारणले नेपालमा औषधी नियमन “कानुनी रूपमा उपस्थित, तर नीतिगत रूपमा अधूरो” जस्तो देखिन्छ।
२) Legal Gap Mapping
A. कानुनी/नियामक ढाँचामा भएको व्यवहारिक अनमेल
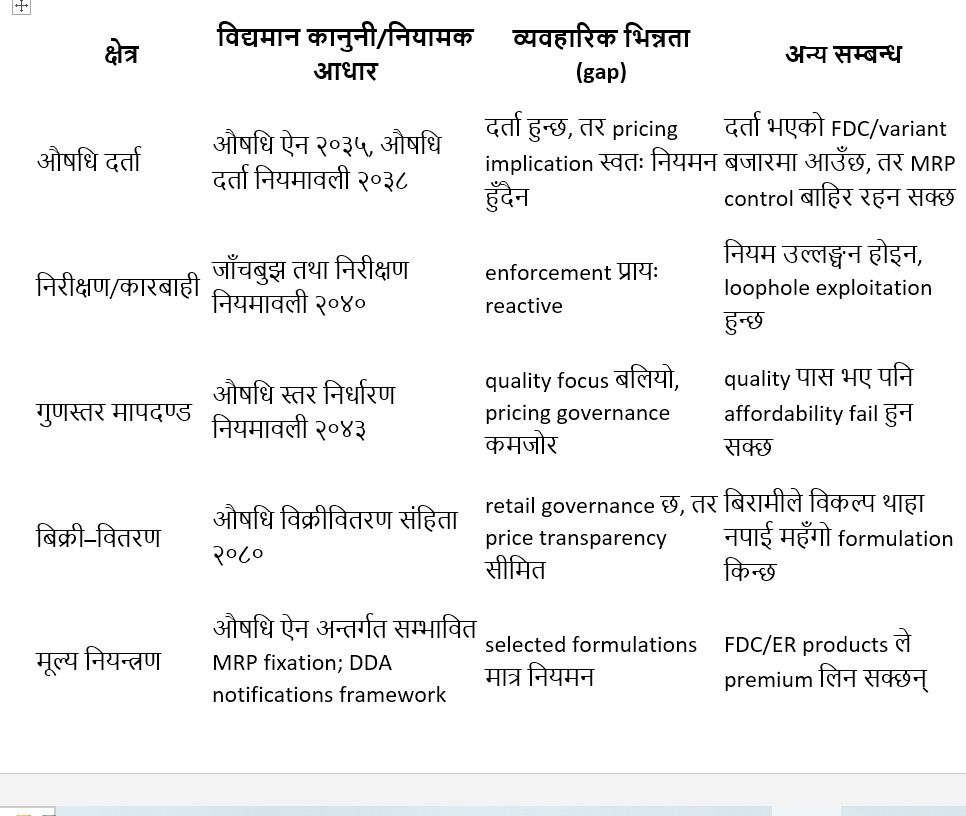
B. खास कानुनी अनमेल
१. Formulation parity को अभाव
कानुन र regulatory tools ले औषधी नियमनको ढाँचा दिएको छ, तर एउटै therapeutic class भित्रका सबै clinically substitutable formulations लाई समान रूपमा price-governed गर्ने स्पष्ट व्यवस्था कमजोर छ। यसको अर्थ single-ingredient product regulate हुन सक्छ, तर FDC वा extended-release variant regulate नहुन सक्छ। यही तपाईंको manuscript को केन्द्रीय gap हो।
२. Mandatory revision mechanism को अभाव
कानुनी संरचनाले price setting सम्भव बनाउँछ, तर revision को frequency, criteria, transparency, stakeholder process र evidence base स्पष्ट institutionalized छैन। यसले पुरानो MRP list लाई market reality सँग disconnect गराउँछ।
३. Pricing law र registration law बीच disconnect
औषधी दर्ता नियमावलीले product लाई बजार प्रवेश दिन सक्छ, तर pricing control स्वतः trigger हुँदैन। त्यसैले दर्ता प्रक्रिया regulatory gateway भए पनि affordability safeguard हुँदैन। यो registration-to-pricing disconnect formulation arbitrage को कानुनी आधारभूत space हो।
४. Consumer information protection कमजोर
औषधी विक्रीवितरण र प्रचार नियन्त्रणका साधन भए पनि retail point मा बिरामीलाई “यो regulated विकल्प हो/यो unregulated premium formulation हो” भन्ने पारदर्शिता कमजोर छ। त्यसैले market choice वास्तविक अर्थमा informed choice हुँदैन।
५. Proactive market surveillance भन्दा complaint-led governance
कानुनमा निरीक्षणको आधार भए पनि व्यवहारमा recall, urgent notices, suspension जस्ता प्रतिक्रियात्मक कदम बढी देखिन्छन्। Pricing distortions भने प्रायः कानून उल्लङ्घन गरेर होइन, कानूनको खाली ठाउँ प्रयोग गरेर हुने भएकाले traditional inspection मात्र पर्याप्त हुँदैन।
C. निश्कर्ष
“नेपालमा औषधी नियमनको मूल कानुनी ढाँचा औषधिको गुणस्तर, दर्ता, बिक्री–वितरण र अनुगमन सुनिश्चित गर्न पर्याप्त आधार प्रदान गर्छ; तर formulation-level price equivalence, नियमित मूल्य पुनरावलोकन, therapeutic substitutability र बिरामीकेन्द्रित affordability protection जस्ता पक्षहरूमा कानुनी तथा नीतिगत रिक्तता बाँकी छ। यही रिक्तताले fixed-dose combinations र modified-release formulations जस्ता उत्पादनहरूलाई नियमनको औपचारिक दायराभन्दा बाहिर उच्च मूल्यमा बजार विस्तार गर्ने अवसर दिन्छ।”
D. नीतिगत सुधारका बुँदा
नेपालका विद्यमान कानुन/नियमको आधारमा पनि तलका सुधारहरू सम्भव देखिन्छन्:
- Therapeutic class-based pricing framework
केवल molecule होइन, substitutable formulations समेत हेर्ने। - Mandatory periodic MRP revision
१–२ वर्षमा evidence-based review बाध्यकारी बनाउने। - Registration-to-pricing linkage
नयाँ FDC/variant दर्ता हुँदा affordability review पनि हुने। - Retail transparency rule
फार्मेसीमा cheaper equivalent जानकारी अनिवार्य गर्ने। - Proactive surveillance + promotion oversight
केवल recall होइन, नियमित market intelligence र promotional audit सुरु गर्ने।
अन्तिम निष्कर्ष
नेपालको समस्या “औषधी नियमन छैन” भन्ने होइन; समस्या “नियमन आंशिक, स्थिर, र formulation-sensitive छैन” भन्ने हो।
यही कारणले कानुनको उपस्थितिबीच पनि market actors ले price-controlled space बाट unregulated formulations तर्फ सर्न सक्ने संरचनागत अवसर पाउँछन्।
कानुनी तथा नीतिगत सन्दर्भ
नेपालको औषधी नियमन प्रणालीको प्रमुख कानुनी आधार औषधी ऐन, २०३५ हो, जसले औषधिको उत्पादन, आयात, दर्ता, वितरण तथा गुणस्तर सुनिश्चित गर्ने अधिकार राज्यलाई प्रदान गर्दछ। यस ऐन अन्तर्गत Department of Drug Administration (DDA) लाई केन्द्रीय नियामक निकायका रूपमा स्थापित गरिएको छ।
यसलाई सहयोग गर्ने नियमावलीहरू—जस्तै औषधी दर्ता नियमावली, २०३८; औषधी निरीक्षण नियमावली, २०४०; औषधी स्तर निर्धारण नियमावली, २०४३; तथा औषधि विक्रीवितरण संहिता, २०८०—ले औषधी आपूर्ति शृङ्खलाको विभिन्न चरणहरूमा नियमनको कार्यान्वयन ढाँचा निर्धारण गर्छन्।
यस कानुनी संरचना अन्तर्गत सरकारले सार्वजनिक हितमा औषधीको मूल्य नियन्त्रण गर्ने अधिकार राख्दछ, जसमा सरकारी राजपत्रमार्फत अधिकतम खुद्रा मूल्य (MRP) निर्धारण गर्ने व्यवस्था पनि समावेश छ। तथापि, व्यवहारमा नेपालमा मूल्य नियमन सीमित र अनियमित रूपमा लागू हुने गरेको देखिन्छ, जुन मुख्यतः केही चयनित एकल-सक्रिय तत्व (single-ingredient) औषधिहरूमा मात्र केन्द्रित छ। यसले बजारको सानो भागमा मूल्य नियन्त्रण गर्न सहयोग पुर्याए पनि, समग्र औषधि बजारलाई समेट्ने व्यापक र नियमित मूल्य नियमन प्रणालीको विकास हुन सकेको छैन।
नेपालको औषधी नियमन प्रणालीको एक प्रमुख कमजोरी भनेको formulation स्तरमा मूल्य समानता सुनिश्चित गर्ने स्पष्ट कानुनी व्यवस्था नहुनु हो। MRP प्रायः विशिष्ट molecule र dosage form मा मात्र लागू हुन्छ, जबकि fixed-dose combinations (FDCs) र modified-release formulations—यद्यपि चिकित्सकीय रूपमा प्रतिस्थापनयोग्य हुन सक्छन्—अधिकांश अवस्थामा मूल्य नियन्त्रणको दायराभन्दा बाहिर रहन्छन्। यसले एउटै उपचार वर्गभित्र विभिन्न formulation हरूलाई फरक मूल्य संरचनामा सञ्चालन हुने अवस्था सिर्जना गर्दछ।
यसैगरी, मूल्य पुनरावलोकनका लागि अनिवार्य, पारदर्शी तथा प्रमाणमा आधारित (evidence-based) प्रणालीको अभाव रहेको देखिन्छ। निर्धारित MRP सूचीहरू समयानुसार अद्यावधिक नहुँदा बजार अवस्था, मुद्रास्फीति, उत्पादन लागत तथा नयाँ formulation हरूसँग मेल नखाने स्थिति उत्पन्न हुन्छ। यसले मूल्य नियमनलाई स्थिर (static) बनाउँदै, उद्योगलाई नियमन बाहिर रहेका वैकल्पिक formulation विकास र विस्तार गर्न प्रोत्साहन दिन्छ।
यद्यपि औषधी दर्ता, गुणस्तर नियन्त्रण, निरीक्षण तथा भ्रामक प्रचार नियन्त्रणका लागि कानुनी संरचना उपलब्ध छन्, दर्ता प्रणाली र मूल्य नियमनबीचको समन्वय कमजोर देखिन्छ। नयाँ formulation हरू, विशेषगरी FDCs, दर्ता प्रक्रियाबाट बजारमा प्रवेश गर्न सक्छन्, तर ती स्वतः मूल्य नियमनको दायरामा समावेश हुँदैनन्। फलस्वरूप, बजार प्रवेश (registration) र affordability protection बीचको सम्बन्ध सुदृढ छैन।
सेवा प्रदान हुने स्तरमा (point of care) पनि थप समस्या देखिन्छ। यद्यपि औषधी विक्रीवितरण र फार्मेसी अभ्यास सम्बन्धी मापदण्डहरू लागू छन्, मूल्य पारदर्शिता र बिरामीलाई जानकारी उपलब्ध गराउने प्रणाली सीमित छ। धेरैजसो अवस्थामा औषधि छनोट चिकित्सकको सिफारिस र बजार प्रवर्द्धनद्वारा प्रभावित हुन्छ, जसले बिरामीको विकल्प सीमित बनाउँछ र उच्च मूल्यका औषधिहरूमा निर्भरता बढाउँछ।
समग्रमा, नेपालको औषधी नियमन प्रणालीलाई आंशिक शासन संरचना (partial governance architecture) का रूपमा बुझ्न सकिन्छ—जहाँ कानुनी अधिकार र संस्थागत संरचना भए पनि, दायरा, समन्वय र अद्यावधिक प्रणालीको कमजोरीले यसको प्रभावकारिता सीमित बनाएको छ। विशेषतः formulation-समावेशी मूल्य नियमन, नियमित पुनरावलोकन प्रणाली, र दर्ता–मूल्य समन्वयको अभावले यस्तो अवस्था सिर्जना गरेको छ जहाँ बजारका actors हरूले कानुनी दायराभित्रै रहेर यसको प्रभावलाई परोक्ष रूपमा छल्न सक्छन्।
यस सन्दर्भले नेपालमा औषधि मूल्य नियमन र बजार व्यवहारबीचको सम्बन्ध बुझ्न तथा formulation-आधारित मूल्य अन्तरहरू विश्लेषण गर्न आधार प्रदान गर्दछ।
चर्चा (Cross-sector governance integration)
यस अध्ययनका निष्कर्षहरू औषधी क्षेत्रमै सीमित नभई नेपालका अन्य सार्वजनिक स्वास्थ्य नियमन क्षेत्रहरू—विशेषतः खाद्य सुरक्षा प्रणाली—सँग पनि गहिरो रूपमा मेल खान्छन्। दुवै क्षेत्रमा एउटा समान संरचनात्मक विशेषता देखिन्छ: कानुनी अधिकार र संस्थागत संरचना त स्थापित छन्, तर नियमनको दायरा अपूर्ण, अद्यावधिक प्रणाली कमजोर, र कार्यान्वयन असमान।
औषधी क्षेत्रमा यो अवस्था चयनात्मक MRP नियमन, formulation-आधारित असमान दायरा, र नियमित मूल्य पुनरावलोकन प्रणालीको अभावका रूपमा देखिन्छ। त्यसैगरी खाद्य सुरक्षा प्रणाली—जसको आधार Food Act 1966 र कार्यान्वयन Department of Food Technology and Quality Control मार्फत हुन्छ—संस्थागत विखण्डन, अनौपचारिक बजारको आंशिक समेटाइ, र प्रतिक्रियात्मक अनुगमन प्रणाली जस्ता समस्याबाट प्रभावित देखिन्छ।
यी दुवै क्षेत्रको तुलना गर्दा स्पष्ट हुन्छ कि नेपालमा नियमनका चुनौतीहरू कुनै एक क्षेत्रमा सीमित छैनन्, बरु समग्र शासन प्रणालीको संरचनात्मक विशेषता (systemic governance pattern) हुन्। यस्तो अवस्थामा, नियमनका सीमाहरू नै बजारका actors हरूका लागि रणनीतिक अवसर बन्ने गर्छन्।
राजनीतिक अर्थशास्त्रको दृष्टिकोणबाट हेर्दा, दुवै क्षेत्रमा partial regulation अन्तर्गत adaptive market behaviour देखिन्छ। औषधि क्षेत्रमा उत्पादकहरूले MRP नियमनबाट बाहिर रहेका formulation (जस्तै FDCs, modified-release) तर्फ सर्ने रणनीति अपनाउँछन्। खाद्य क्षेत्रमा भने अनौपचारिक उत्पादन, कमजोर अनुपालन, र नियमन बाहिर रहेका बजारहरूको विस्तार देखिन्छ।
महत्वपूर्ण कुरा के हो भने यी व्यवहारहरू प्रायः कानुन उल्लङ्घन गरेर होइन, कानुनको दायराभित्रका खाली ठाउँ (regulatory gaps) प्रयोग गरेर हुने गर्छन्। यसले देखाउँछ कि समस्या enforcement मात्र होइन, नियमनको डिजाइन र दायरा सँग सम्बन्धित छ।
दुवै क्षेत्रमा देखिने अर्को समानता भनेको नियमनको अपूर्ण दायरा (incomplete coverage) हो। औषधी क्षेत्रमा formulation-level pricing समावेश छैन भने खाद्य क्षेत्रमा informal sector पूर्ण रूपमा नियमनमा आएको छैन। यसले regulated र unregulated बजारबीच स्पष्ट विभाजन सिर्जना गर्छ।
त्यसैगरी, दुवै क्षेत्रमा समयअनुसार अद्यावधिक (revision) गर्ने संस्थागत प्रणाली कमजोर छ। स्थिर नियमनले गतिशील बजार परिवर्तनसँग तालमेल गर्न सक्दैन, जसले गर्दा नियमनको प्रभाव क्रमशः घट्दै जान्छ।
उपभोक्ता स्तरमा पनि सूचना असमानता (information asymmetry) दुवै क्षेत्रमा साझा समस्या हो। बिरामी वा उपभोक्ताले मूल्य, गुणस्तर वा विकल्पबारे पर्याप्त जानकारी पाउँदैनन्, र निर्णय प्रायः बीचका actors (जस्तै prescriber वा vendor) द्वारा प्रभावित हुन्छ।
यी सबै समानताहरूले एउटा महत्वपूर्ण निष्कर्ष दिन्छन्:
नियमनको प्रभावकारिता केवल कानुनको अस्तित्वमा निर्भर हुँदैन; यो नियमनको दायरा, बजार संरचना, र actor incentive बीचको समन्वयमा निर्भर हुन्छ।
नेपालका लागि यसले संकेत गर्छ कि औषधि मूल्य नियमन सुधार केवल एक क्षेत्रको मुद्दा होइन, बरु समग्र नियामक प्रणाली सुधार (regulatory system strengthening) सँग सम्बन्धित छ। यसको लागि:
- दायरा विस्तार गर्ने
- नियमित र पारदर्शी revision प्रणाली विकास गर्ने
- preventive र risk-based नियमन अपनाउने
- र बजार व्यवहारलाई ध्यानमा राखेर नीति डिजाइन गर्ने
आवश्यक छ।
अन्ततः, नेपालले देखाएको अनुभवले अन्य LMIC हरूका लागि पनि महत्वपूर्ण पाठ दिन्छ: आंशिक नियमनले बजारलाई नियमनअनुसार होइन, नियमनको सीमा अनुसार अनुकूलित हुन प्रोत्साहन दिन्छ।
सम्पर्क इमेल : [email protected]